Liaison chimique
1) Donnez la structure en logettes des orbitales de la couche électronique externe (soit les orbitales susceptibles d'accueillir des électrons dans leur état fondamental) des atomes C et Si. Cocher la(les) bonne(s) réponse(s) :
A. Pour le carbone :
B. Pour le silicium :
Donnez la structure en logettes des électrons hébergés par les orbitales, disponibles après hybridation, dans la couche électronique externe des atomes C et Si :
C. Pour le carbone :
D. Pour le silicium :
E. Quelles règles ou lois (de Lavoisier, Pauli, Arrhénius, Hund ou Mendéléev … ou encore : stabilité énergétique de l'atome) sont respectées ou non dans les structures présentées ci-dessus ?
2) Donnez la structure de Lewis, les charges formelles (sans oublier les PEL ni les éventuels électrons célibataires) et la polarité (éventuelle) de :
A. NO (Cocher la(les) bonne(s) réponse(s)) :
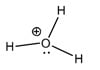
B. Ion Hydronium (Cocher la (les) bonne(s) réponse(s))
3) Dans ClO4- l'atome de chlore est hybridé :
Actuellement veuillez naviguer du dernier exercice vers le premier (flèche gauche uniquement).


 (Ariane Lejeune) Copyright: UCL - FUNDP © 2012–
(Ariane Lejeune) Copyright: UCL - FUNDP © 2012–
 Cette oeuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution - Pas d'Utilisation Commerciale - Partage à l'Identique 2.0 Belgique.
Cette oeuvre est mise à disposition selon les termes de la Licence Creative Commons Attribution - Pas d'Utilisation Commerciale - Partage à l'Identique 2.0 Belgique.